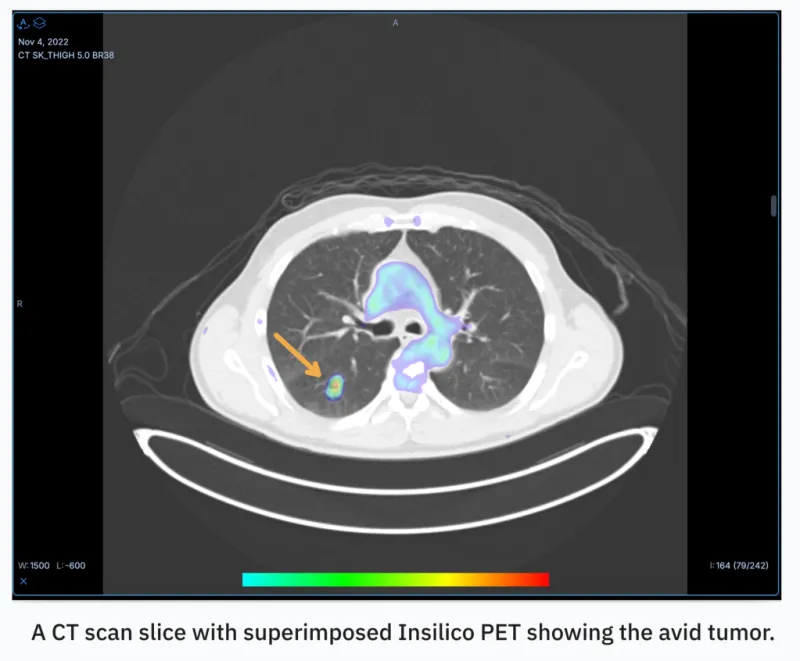
Позитронно-эмиссионная томография (ПЭТ) — это сложная процедура. Хотя эти сканы помогают врачам выявлять рак и отслеживать его распространение, сам процесс зачастую доставляет пациентам немало неудобств. Подготовка включает четырех-шестичасовое голодание перед визитом в больницу. Для жителей отдаленных районов, где нет ПЭТ-сканеров, это может обернуться настоящей логистической проблемой.
По прибытии в клинику пациентам вводят радиоактивный материал, после чего следует часовое ожидание, пока он распределится по организму. Затем пациента помещают в ПЭТ-сканер, где необходимо пролежать неподвижно около 30 минут для получения изображения. После процедуры требуется избегать контактов с пожилыми людьми, детьми и беременными женщинами до 12 часов, поскольку пациент остается слегка радиоактивным.
Еще одним ограничением является концентрация ПЭТ-сканеров в крупных городах. Это связано с тем, что радиоактивные трассеры производятся в близлежащих циклотронах — компактных ядерных машинах — и должны быть использованы в течение нескольких часов. Такое условие ограничивает доступность ПЭТ-диагностики в сельских и региональных больницах.
Но что, если бы можно было использовать искусственный интеллект для преобразования КТ-сканов, которые гораздо доступнее и дешевле, в ПЭТ-изображения? Именно такую задачу решает стартап RADiCAIT. Компания, выделившаяся из Оксфордского университета, привлекла 1,7 миллиона долларов предварительного финансирования. RADiCAIT, базирующаяся в Бостоне и являющаяся финалистом конкурса Startup Battlefield на TechCrunch Disrupt 2025, готовится к привлечению 5 миллионов долларов для проведения клинических испытаний.
«Мы взяли наиболее ограниченное, сложное и дорогостоящее решение в медицинской визуализации — ПЭТ — и заменили его наиболее доступным, простым и недорогим — КТ», — сообщил генеральный директор RADiCAIT Шон Уолш.
Секрет RADiCAIT кроется в ее фундаментальной модели — генеративной глубокой нейронной сети, разработанной в 2021 году в Оксфордском университете командой под руководством соучредителя и главного медицинского информационного директора компании Регента Ли. Модель обучается путем сравнения КТ- и ПЭТ-сканов, сопоставления их и выявления закономерностей во взаимосвязи.
Главный технолог RADiCAIT Сина Шахандех описывает этот процесс как соединение «различных физических явлений» путем перевода анатомической структуры в физиологическую функцию. Затем модель направляется на детальное изучение конкретных особенностей сканов, таких как определенные типы тканей или аномалии. Это сфокусированное обучение повторяется многократно с различными примерами, чтобы модель могла идентифицировать клинически значимые закономерности.
Финальное изображение, которое предоставляется врачам для анализа, создается путем объединения нескольких взаимосвязанных моделей. Шахандех сравнивает этот подход с AlphaFold от Google DeepMind, ИИ, который революционизировал предсказание структуры белков: обе системы учатся преобразовывать один тип биологической информации в другой.
Уолш утверждает, что команда RADiCAIT может математически доказать статистическую схожесть сгенерированных ПЭТ-изображений с реальными химическими ПЭТ-сканами. «Наши испытания показывают, что врачи и онкологи принимают те же решения, независимо от того, предоставлены ли им химические ПЭТ-сканы или наши ПЭТ-изображения, сгенерированные ИИ», — отметил он.
RADiCAIT не претендует на полную замену ПЭТ-сканирования в специфических терапевтических целях, например, при радионклейдной терапии, которая уничтожает раковые клетки. Однако для диагностики, стадирования и мониторинга заболеваний технология RADiCAIT может сделать традиционные ПЭТ-сканы устаревшими.
«Из-за высокой степени ограниченности системы спрос на диагностику и тераностику превышает предложение», — сказал Уолш, имея в виду медицинский подход, сочетающий диагностическую визуализацию (ПЭТ) с таргетной терапией (например, при лечении рака). «Мы стремимся удовлетворить этот спрос в области диагностики. Сами ПЭТ-сканеры должны будут справляться с растущими потребностями в тераностике».
RADiCAIT уже начала пилотные клинические испытания для диагностики рака легких совместно с крупными медицинскими центрами, такими как Mass General Brigham и UCSF Health. В настоящее время стартап проходит процедуру получения одобрения FDA, что является дорогостоящим и трудоемким процессом, для которого и привлекается раунд финансирования в размере 5 миллионов долларов. После получения одобрения следующим шагом станут коммерческие пилотные проекты для демонстрации рыночной жизнеспособности продукта. RADiCAIT планирует применить аналогичный подход — пилотные клинические исследования, клинические испытания, коммерческие пилоты — для случаев колоректального рака и лимфомы.
Шахандех подчеркнул, что подход RADiCAIT к использованию ИИ для получения достоверных данных без сложностей и дороговизны традиционных тестов «широко применим». «Мы изучаем возможности расширения применения в других областях радиологии», — добавил он. «Ожидайте аналогичных инноваций, связывающих области от материаловедения до биологии, химии и физики, везде, где можно изучить скрытые закономерности природы».